Foire aux questions sur le règlement UE relatif aux dispositifs médicaux (MDR)
Le nouveau règlement de l’Union européenne relatif aux dispositifs médicaux (MDR) visant à améliorer l’innocuité clinique est entré intégralement en vigueur le 26 mai. Contrairement aux directives, les règlements n’ont pas à être transposés dans le droit national.
Le règlement relatif aux dispositifs médicaux concerne tous les dispositifs médicaux vendus en Europe, y compris les produits de Formlabs. Notre article de blog répond aux questions les plus fréquemment posées sur le nouveau règlement relatif aux dispositifs médicaux et sur la manière dont il affecte Formlabs ainsi que nos clients.
Qu'est-ce qu’un dispositif médical ?
On définit un dispositif médical comme « tout instrument, appareil, dispositif, logiciel, implant, agent, matériau ou autre élément » conçu pour être utilisé pour le diagnostic, la prévention ou le traitement des maladies et des blessures.
Parmi les produits de Formlabs, lesquels sont des dispositifs médicaux ?
| Dispositif médical | Classe | Fabricant |
|---|---|---|
| Guide chirurgical | Classe I | Formlabs |
| Custom Tray Resin | Classe I | Formlabs |
| IBT Resin | Classe I | Formlabs |
| Dental LT Clear Resin (V2)* | Classe IIa | Formlabs |
| Dental SG Resin | Classe I | Tiers |
| Dental LT Clear Resin V1 | Classe IIa | Tiers |
| Temporary CB Resin | Classe IIa | Tiers |
| Permanent Crown Resin | Classe IIa | Tiers |
| Denture Base Resin | Classe IIa | Tiers |
| Denture Teeth Resin | Classe IIa | Tiers |
*pas encore disponible en Europe
Comment s’assurer que les dispositifs médicaux de Formlabs utilisés soient conformes au règlement sur les dispositifs médicaux (MDR) à compter du 26 mai 2021 ?
Dispositifs de classe I : les changements s’appliqueront uniquement aux dispositifs fabriqués après l e 26 mai 2021.
Conformément à l’article 120, paragraphe 4 du règlement de l’Union européenne sur les dispositifs médicaux, les dispositifs légalement mis sur le marché en application de la directive 93/42/CEE (dispositifs médicaux) avant le 26 mai 2021 pourront continuer à être mis à disposition sur le marché ou mis en service jusqu’au 27 mai 2025.
Par conséquent, Formlabs certifie que ses dispositifs médicaux de classe I fabriqués avant le 25 mai 2021 et expirant le 25 mai 2023 au plus tard peuvent être utilisés et vendus conformément au règlement de l’Union européenne sur les dispositifs médicaux.
Télécharger la déclaration officielle
Dispositifs de classe IIa : aucun changement jusqu’à 2024* (consultez la déclaration officielle pour obtenir les dates exactes)
Conformément à l’article 120, paragraphe 4 du règlement de l’Union européenne sur les dispositifs médicaux, les dispositifs légalement mis sur le marché en application de la directive 93/42/CEE (MDD) en vertu d'un certificat valide (valide jusqu’au terme de la période indiquée sur le certificat) pourront continuer à être mis à disposition sur le marché ou mis en service jusqu’au 27 mai 2025.
Par conséquent, Formlabs certifie que ses dispositifs médicaux de classe IIa peuvent être utilisés et vendus conformément au règlement de l’Union européenne sur les dispositifs médicaux.
En ce qui concerne les dispositifs médicaux produits par Formlabs après le 26 mai 2021, quels changements seront visibles sur les étiquettes ?
Le marquage inclut le mode d'emploi, la contre-étiquette et toute autre étiquette se trouvant sur la cartouche ou la boîte. Le marquage MDR diffère du marquage MDD dans le sens où celui-ci doit comprendre :
-
Un symbole « MD » (indiquant que le produit est un dispositif médical)
-
Le nom de l’importateur
-
Un IUD (identifiant unique du dispositif)
-
Les modes d’emploi incluant les avantages cliniques, les risques résiduels et autres exigences de l’annexe I
Les produits de Formlabs posséderont des étiquettes conformes au règlement sur les dispositifs médicaux (MDR), le cas échéant. Veuillez noter que, même si le marquage inclut tout les éléments ci-dessus, cela ne signifie pas forcément que le dispositif médical en question satisfait à l’ensemble des conditions requises par le règlement sur les dispositifs médicaux (MDR).
Quelles sont les certifications nécessaires ?
Les dispositifs de classe I n’ont besoin d'aucune certification, uniquement d’une déclaration de conformité, qui constitue l’auto-certification du fabricant. Ces dispositifs doivent quand même être fabriqués et étiquetés conformément au règlement.
Les dispositifs de classe IIa nécessitent un certificat CE émis par un organisme agréé ainsi qu’une déclaration de conformité.
Que signifient ces changements pour Formlabs ?
Ces changements ont différentes significations pour les dispositifs de Formlabs.
Dispositifs de classe I de Formlabs
-
Les dispositifs de classe I passeront de produits MDD à produits MDR, une fois que le stock aura été épuisé.
-
Formlabs possédera une déclaration de conformité MDR.
-
Les produits possèderont des modes d’emploi et des marquages conformes MDR.
Dispositifs de classe IIa de Formlabs
-
Quand Dental LT Clear Resin V2 sera disponible en Europe, elle possèdera un certificat CE MDR et le système de qualité de Formlabs sera certifié MDR.
Dispositifs de classe IIa tiers
-
Les dispositifs de classe IIa garderont un certificat MDD et aucun changement ne sera effectué jusqu’à expiration du certificat (en fonction du certificat, pas plus tard que le 26 mai 2024)
Quand doit arriver la déclaration de conformité MDR de Formlabs ?
Tous les dispositifs médicaux de classe I distribués par Formlabs et fabriqués après le 26 mai 2021 ont besoin d'une nouvelle déclaration de conformité. Les dispositifs de classe I de Formlabs possèderont une déclaration de conformité MDR pour les lots fabriqués après le 25 mai 2021.
Est-ce que la déclaration de conformité MDR s’applique aux résines et aux imprimantes ?
La déclaration de conformité MDR s’applique à toutes les résines de classe I vendues par Formlabs. Cependant, le règlement sur les dispositifs médicaux (MDR) ne s’applique pas aux imprimantes de Formlabs. Les imprimantes ont une déclaration de conformité en vertu d’une législation différente.
Quelles sont les exigences pour les clients dentaires de Formlabs ?
En vertu du règlement sur les dispositifs médicaux (MDR) les laboratoires et cabinets dentaires sont désormais des fabricants. Tout produit qui constitue un dispositif médical doit être fabriqué conformément à un système de qualité défini.
Les fabricants doivent :
-
Satisfaire à l’ensemble des exigences de performance et de sécurité générale
-
Respecter l’ensemble des exigences post-commercialisation
-
S’enregistrer en tant que fabricant de dispositif (spécifique au territoire)
-
Rédiger une déclaration Annexe XIII (semblable à la déclaration de conformité)
-
Nommer une personne chargée de la conformité réglementaire
Comment Formlabs peut-elle aider les clients à répondre aux obligations du règlement sur les dispositifs médicaux (MDR) ?
Formlabs peut aider les clients à satisfaire aux exigences de performance et de sécurité générale (annexe I du règlement sur les dispositifs médicaux [MDR]) en présentant sur demande :
-
Certificat d’analyse ⇒ Illustre la qualité et le contrôle des lots
-
Certificat de conformité ⇒ Illustre la conformité avec l’annexe I
Documents supplémentaires permettant de démontrer la conformité :
-
Déclaration de conformité des dispositifs médicaux : téléchargez les documents dans la partie « Downloads » (téléchargements) pour chaque indication (le cas échéant)
-
Fiche technique : téléchargez les documents dans la partie « Downloads » (Téléchargements) pour chaque indication
-
FDS : téléchargez les documents en bas de page
-
Preuve que les dispositifs de classe I sont conformes MDR (fabriqués avant le 26 mai)
En localisant les équipements et matériaux, l’outil en ligne Dashboard de Formlabs vous assiste avec les exigences relatives aux documents de l’article 5.
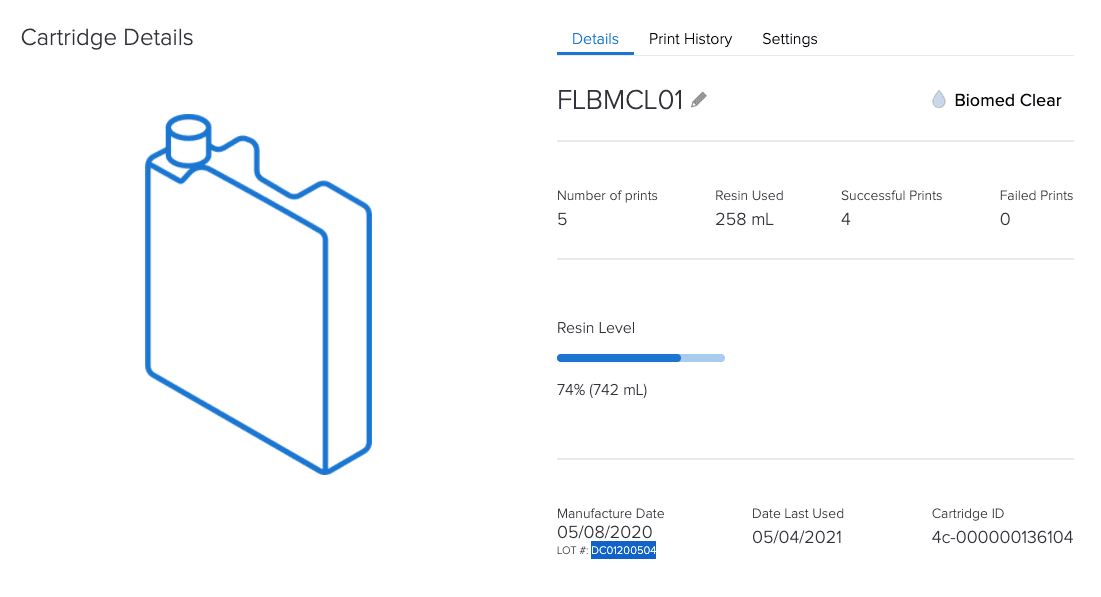
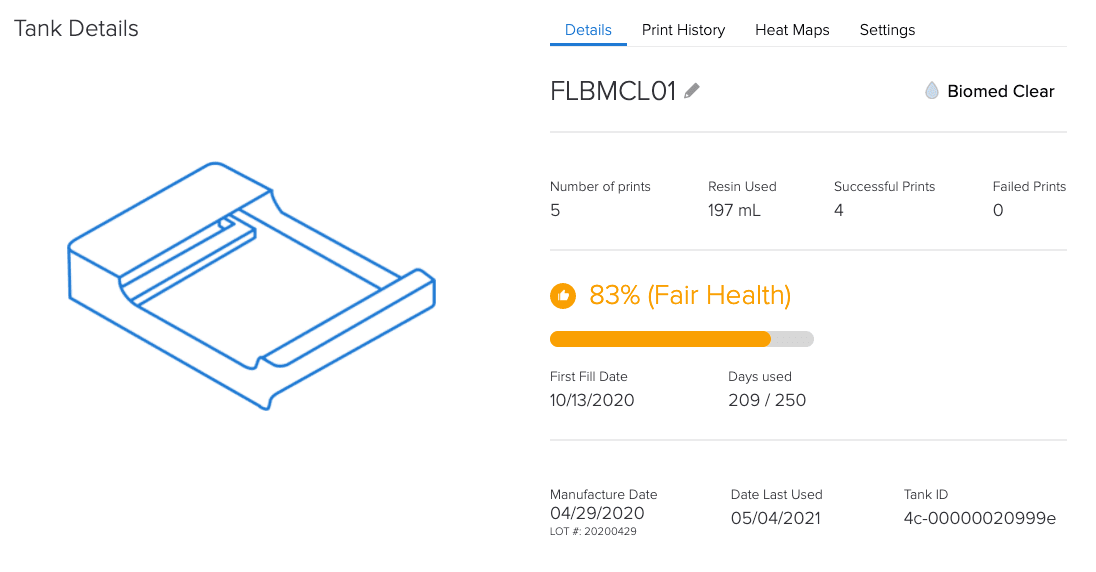
Dans quelle mesure un écosystème contrôlé de Formlabs est-il un avantage en vertu du règlement sur les dispositifs médicaux (MDR) ?
Étant donné que tous les clients dentaires (laboratoires et cabinets) et toutes les institutions médicales doivent se conformer à l’ensemble des exigences du règlement sur les dispositifs médicaux (MDR), posséder un système contrôlé offre confiance et de conformité.
-
Un système contrôlé offre une assurance de conformité complète avec l’annexe I pour l’imprimante et le matériau.
-
Une évaluation clinique soutenant le matériau et l’imprimante.
-
La conformité sous la forme de documents pour chaque lot et de documentation numérique.
Les imprimantes et matériaux Formlabs ainsi que les produits qui y sont associés se conforment à diverses normes de qualité et de sécurité dans différentes juridictions. Des informations supplémentaires sont disponibles ici.
Apprenez-en plus sur le MDR
Regardez notre webinaire sur le MDR, dans lequel Sam Murray, directeur des services Assurance qualité et Affaires réglementaires à Formlabs, vous donnera un aperçu détaillé du nouveau règlement et de son impact sur les clients Formlabs.